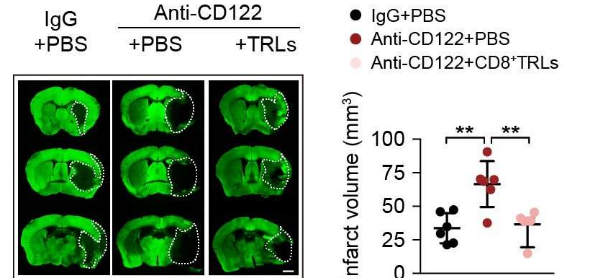
2月20日积极的养育方式可以降低儿童患肥胖症的风险
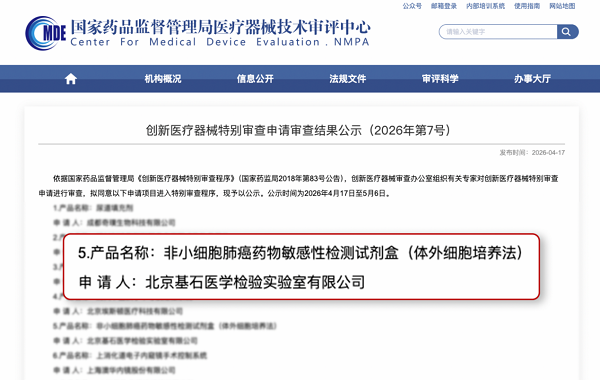
2026年4月17日,国家药品监督管理局医疗器械技术审评中心(CMDE)发布《创新医疗器械特别审查申请审查结果公示(2026年第7号)》,由北京基石医学检验实验室有限公司(基石生命旗下)自主研发的非小细胞肺癌药物敏感性检测试剂盒(体外细胞培养法)成功入选,拟进入创新医疗器械特别审查程序。这是国内首个基于体外细胞培养法的非小细胞肺癌药物敏感性检测试剂盒,标志着我国类器官药敏检测方法正式进入国家临床应用评审阶段。
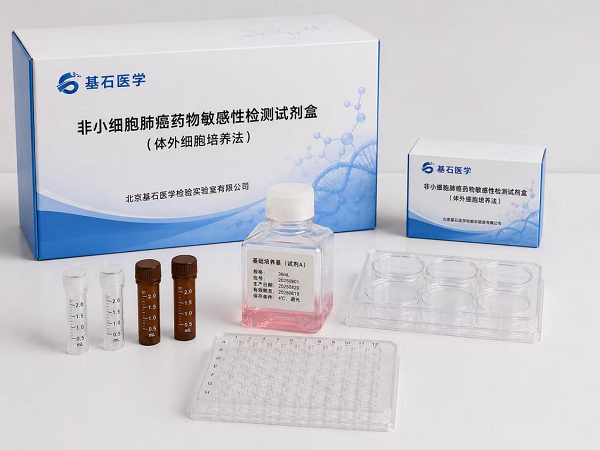
一、里程碑式突破:国内首款自组装肿瘤类器官肺癌药敏检测产品
肺癌是全球第一位致死恶性肿瘤,其中,非小细胞肺癌(NSCLC)作为肺癌的主要类型,占比超80%,患者对化疗、靶向、免疫药物的个体差异较大,传统基因检测难以全面预测药物疗效,临床亟需更直接的药敏检测工具。
本次入选的试剂盒,是国内首个获批进入国家创新通道的、基于患者原代肿瘤细胞体外培养技术的非小细胞肺癌药敏检测产品,一举填补国内同赛道技术与产品空白,实现领域突破性创新。其核心技术依托基石生命自主研发的自组装肿瘤类器官(微肿瘤PTC)(Patient-Derived Tumor-like Cell Clusters)原代肿瘤细胞体外培养平台,可实现患者肿瘤细胞的快速扩增与多药物敏感性检测,为临床提供“直接、全面、精准”的用药指导依据。
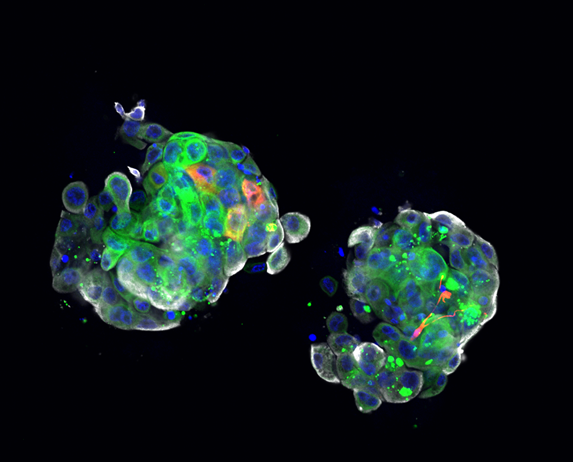
国内首创的技术路径:区别于传统基因检测,该产品直接从患者肿瘤组织中分离原代细胞,构建与患者肿瘤生物学特征高度一致的体外药敏模型,可同时评估化疗、靶向等治疗药物的疗效。
填补临床空白的产品定位:作为国内首个进入创新审查程序的体外细胞培养法药敏检测试剂盒,将为晚期、耐药、多线治疗失败的非小细胞肺癌患者提供全新的个体化用药选择,助力临床从“经验治疗”向“精准药敏指导治疗”跨越。
二、硬核技术支撑:从科研突破到临床转化的关键跨越
该产品的技术核心——自组装肿瘤类器官(微肿瘤PTC)技术,源自北京大学席建忠教授团队的科研成果,基石生命通过多年临床转化,实现了技术的标准化、可规模化应用,为产品的合规化注册奠定了坚实基础。

高成功率与高一致性:技术前期已完成多项临床验证(预实验),非小细胞肺癌建模成功率超90%,药敏检测结果与临床疗效的一致性较高,化疗药物预测准确性88.2%,靶向药物预测准确性89.6%,总体一致性为89%,预测CR/PR组与PD组的准确率高达98.1%具备可靠的临床应用价值。
另一项自组装肿瘤类器官(微肿瘤PTC)指导晚期非小细胞肺癌患者多模态治疗(介入)药物选择的研究中,PTC显著提升了晚期非小细胞肺癌患者介入治疗有效率:PTC指导下的ORR率达到70%,显著高于文献报道的ORR率36.5%-47.5%。
合规化的里程碑进展:本次入选国家创新医疗器械特别审查程序,意味着产品将进入审评“绿色通道”,享受优先审评、专人沟通指导等支持,加速实现从科研服务到合规医疗器械的转化,未来有望成为国内首个获批上市的同类产品。
三、行业影响:推动肿瘤精准医疗规范化发展
创新医疗器械特别审查程序,是国家为鼓励医疗器械创新、加快临床急需产品上市设立的重要机制。该产品的成功入选,不仅是对基石生命技术创新能力的权威认可,更对国内肿瘤精准医疗领域具有里程碑意义:
1.打破技术垄断:此前国内缺乏基于原代细胞培养的合规药敏检测产品,该产品的推进有望打破行业空白,建立国产技术标准,降低患者对进口技术的依赖。
2.规范药敏检测市场:通过国家创新通道的审评监管,推动肿瘤药敏检测从科学研究向医疗器械转化,为临床提供可溯源、可验证的标准化检测工具。
3.惠及广大肺癌患者:产品上市后,将为非小细胞肺癌患者提供更全面的科学用药指导,提升治疗有效率,减少无效治疗,降低治疗副作用,减少患者开支和医疗资源浪费;对晚期、耐药患者尤为重要,他们往往只有一次治疗机会,精准个体化用药能为他们带来新的生存希望。
基石生命将继续全力推进产品的注册申报与临床验证工作,力争早日实现产品上市,助力我国肺癌精准治疗事业高质量发展,让更多患者直接受益于科研成果。
-
到目前为止细胞和基因治疗公司在2021年看到超过$13.6B
2022-12-22 -
新研究表明对心脏最有益的早餐习惯
2022-12-22 -
研究人员对乳房重建结果的看法存在差异
2022-12-22 -
SLFN11 在蛋白质稳态中的监测作用
2022-12-22 -
2022年1月18日整理发布:养脑护脑的八大攻略
2022-12-22 -
7种神奇的草药 可增加快乐荷尔蒙
2022-12-22 -
PSA筛查与降低前列腺癌死亡率的风险有关
2022-12-22 -
与肝癌有关的合成永久化学物质
2022-12-22 -
早起限时进食对减肥更有效
2022-12-22 -
新的产前检查可以减少检测染色体异常的时间和成本
2022-12-22